卒中(stroke)是我国排在第一的高致死高致残的疾病,严重危害了人类的生命健康。近年来的临床上应用药物溶栓和机械取栓治疗急性缺血性卒中,患者死亡率大大降低,但存活的患者却存在不同程度甚至十分严重的神经功能障碍。阐明神经功能障碍的分子病理机制,改善卒中病人预后,是全世界正在努力攻克的一个科学难题。
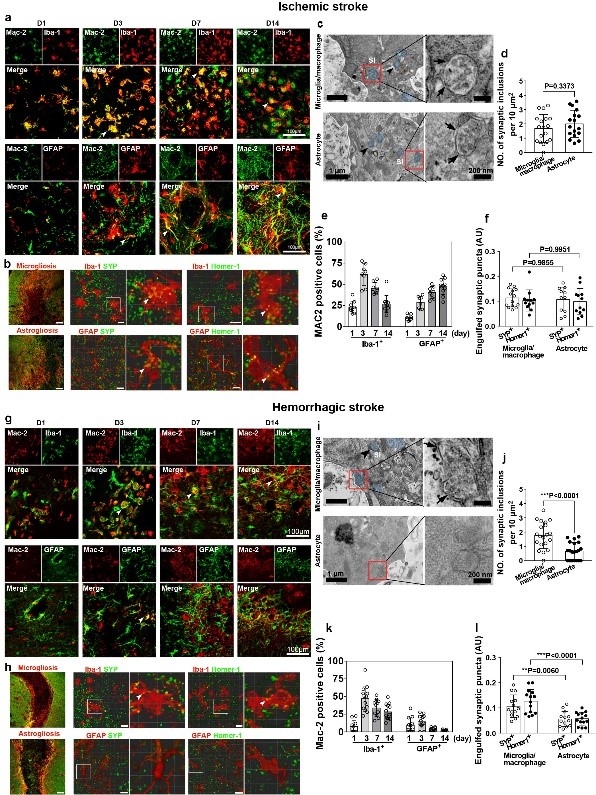
反应性胶质细胞在不同卒中类型中的吞噬功能差异
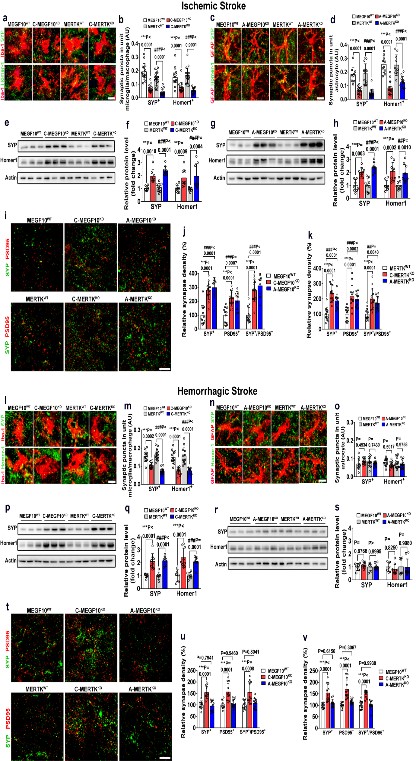
抑制胶质细胞吞噬促进了脑损伤区突触密度
近日,js345线路检测杨国源教授课题组在Nature Communications发表了题为“Stroke-subtype dependent synapse elimination by reactive gliosis in mice”的研究工作。该工作利用啮齿类动物脑血管疾病模型,探索小胶质细胞/巨噬细胞(microglia/macrophage)和星形胶质细胞(astrocyte)在缺血性卒中和出血性卒中修复阶段的突触吞噬情况。研究发现两种胶质细胞在脑缺血(ischemic stroke)小鼠中过度激活从而吞噬神经突触,使得突触丢失影响了疾病预后;而在脑出血小鼠中只有小胶质细胞/巨噬细胞过度激活介导突触吞噬,星形胶质细胞无明显作用。采用条件性基因敲除小鼠。通过免疫电镜、高尔基染色等技术证明了反应性胶质细胞是通过MEGF10/MERTK吞噬通路对胶质增生区域的突触前膜和后膜进行吞噬。单细胞测序分析进一步发现了与缺血性卒中相比,出血性卒中后介导神经突触吞噬的星形胶质细胞亚群数量明显降低。所有这些结果都提示了在卒中修复期,胶质细胞可通过MEGF10和MERTK这两个关键分子吞噬神经突触,导致神经突触丢失和神经环路破坏,最终造成神经功能障碍。
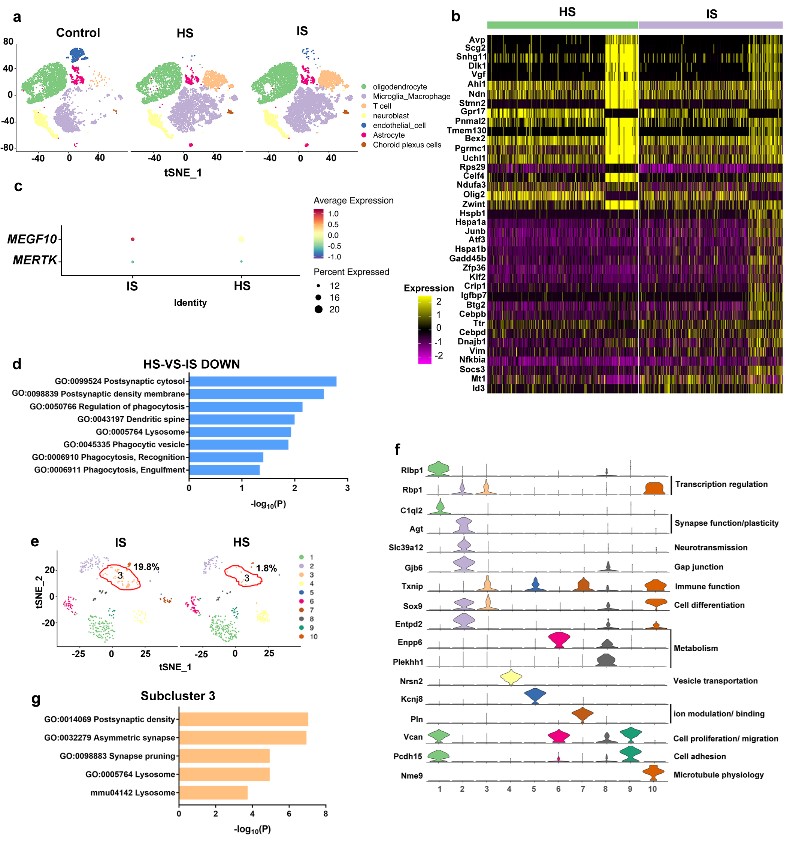
脑出血后介导突触吞噬的星形胶质细胞亚群数量减少
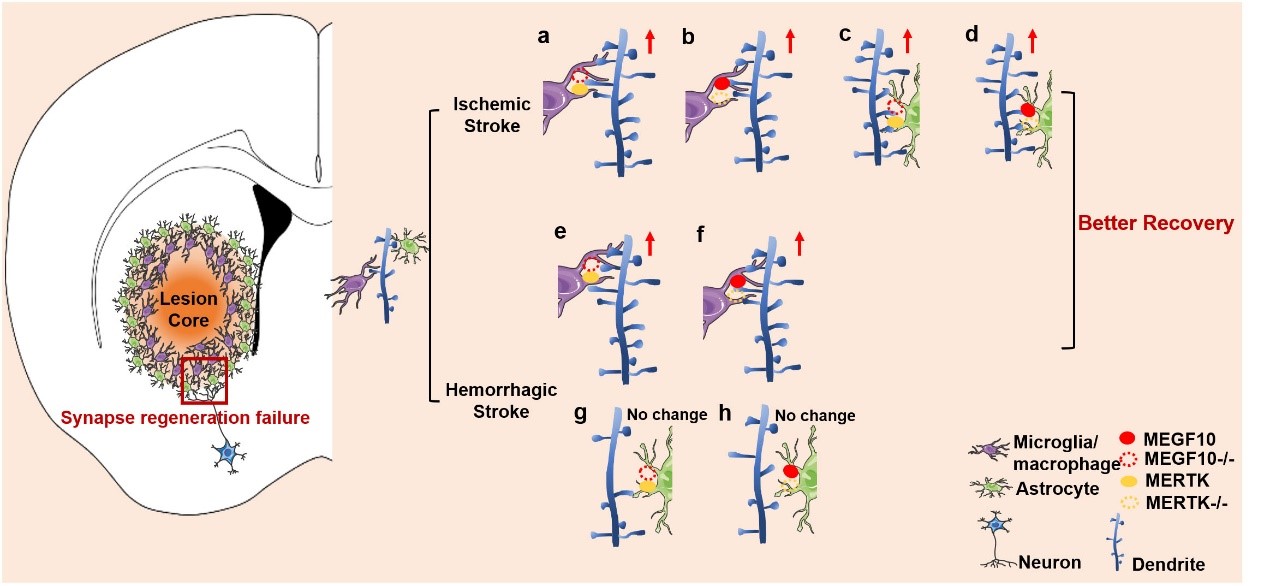
脑损伤后的神经突触再生和神经网络重塑是神经损伤修复的关键,在卒中后1-2周,神经突触再生到达峰值,此时活化增殖的胶质细胞可形成反应性胶质增生区域;胶质增生对于神经突触再生是有益还是有害的,一直都是充满争议的科学问题。杨国源团队的研究证明了小胶质细胞和星形胶质细胞可通过吞噬作用造成神经突触丢失;而抑制胶质细胞吞噬能显著增加损伤周边区的神经突触密度,减轻小鼠脑损伤,改善小鼠的运动和认知功能。鉴于小胶质细胞和星形胶质细胞在不同卒中类型中介导突触吞噬的差异性,针对不同脑损伤病理阶段,开发精准有效治疗策略,将大大促进脑血管病的预后。
js345线路检测博士生施晓婧、硕士生罗龙龙(现在瑞典KTH攻读博士)、js345线路检测医学院附属瑞金医院康复医学科主治医生王继先博士为论文的共同第一作者,韩国科学技术院助理教授Won-Suk Chung、js345线路检测助理教授汤耀辉和讲席教授杨国源为论文的共同通讯作者。该研究工作得到了国家科技部、自然科学基金委、上海市科学技术委员会、上海市教育委员会等项目的支持。
供稿单位:科研与学科办
作者:陶丽宁、黄娟娟
审核:古宏晨
